位置:
学术进展
位置:
学术进展2020年4月,王友军教授课题组的题为“Optical control of CRAC channels using photoswitchable azopy-razoles”的文章在杂志Journal of the American Chemical Society(J. Am. Chem. Soc.April 24. 2020 doi:10.1021/jacs.0c02949)(IF: 14.695)正式被接收。该研究由王友军教授团队,山东大学药学院李敏勇教授团队和美国德州农工大学研究团队共同合作完成。生科院学生郑思思同学为共同第一作者。
在哺乳动物中,钙释放激活钙通道(CRAC通道)介导的钙内流对调控细胞的生理过程有着非常重要的作用,其异常会引发包括联合重症免疫缺陷,神经退行性疾病,心血管疾病等疾病。其中Storkormen综合症由Orai1或STIM1(R304W)的获得性突变引起。因此,调控CRAC通道对治疗相关疾病有着重要意义。光药物学由于其高度的时空可控性及特异性高等优点而被广泛用于精确控制生物活性靶点,如离子通道、受体、酶和核酸等。目前,对CRAC通道的光学操控主要集中于光遗传学激活剂,而对光控抑制剂方面的研究较少。而与我们合作的李敏勇教授团队开发了一系列可以光控改变构象的CRAC通道抑制剂(命名为piCRACs)。
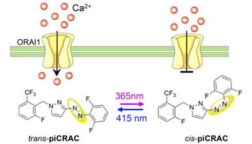
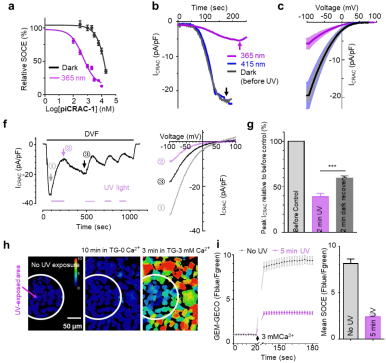
其中的piCRAC-1在经紫外光照射后,可以对CRAC钙信号及CRAC电流有显著的抑制。 该抑制作用具有部分可逆性且有较好的空间分辨率。进一步的测试表明piCRAC1能抑制CRAC通道的下游转录因子NAFT的激活,并可以有效缓解斑马鱼Stormorken综合征模型的相关表型。
本研究为光控CRAC通道抑制剂在人类疾病方面的潜在应用提供了原型工具。
本研究受自然科学基金面上项目NSFC- 91954205及31671492的资助。